免疫治疗的出现给抗肿瘤治疗领域带来了翻天覆地的变化,但受限于肿瘤的免疫抑制环境和肿瘤特异性细胞毒性T淋巴细胞(CTL)的不足,免疫治疗的响应率仍有很大提升空间。
2026年1月7日,,北京大学化学与分子工程学院陈鹏团队在《Nature》期刊上发表了题为《Intratumoural vaccination via checkpoint degradation-coupled antigen presentation》的研究论文,首次提出“降解疫苗”新策略,为攻克癌症免疫耐受难题提供了全新路径。

研究团队巧借“特洛伊木马”之计,设计了一个神奇分子,使其能潜入肿瘤细胞发挥双重效能。这项工作直面临床真实需求,点燃了癌症疫苗疗法的新希望,为解决重大医学问题贡献了独特智慧。
唤醒体内免疫系统的关键:解决癌症疫苗的“瞄准”痛点
面对全球沉重的癌症负担,这项研究被视为推动癌症疫苗走向临床的关键拼图。其思路并非传统的“苦苦认脸”,而是直接为肿瘤强行插上一面免疫系统能清晰识别的“攻击旗帜”。
传统癌症疫苗旨在让免疫系统通过识别肿瘤特异性抗原来攻击癌细胞。但这面临“瞄准困境”:许多肿瘤细胞缺乏独特的抗原“身份标签”,同时高表达PD-L1等免疫抑制蛋白(穿上“防护服”),成为“冷肿瘤”。这导致免疫系统如同患上“脸盲症”,无法有效识别与攻击。
北大团队着力解决的,正是如何让免疫系统“看见”并攻击这些擅长“隐身”的肿瘤。
研究的核心创新在于思维转换——不再寻找难以捉摸的“身份标签”,转而直接插入通用的“攻击旗帜”。研究人员利用化学工具,设计了一种名为“瘤内疫苗嵌合体”(iVAC)的新型分子,强行给肿瘤打上免疫系统必然认识的醒目标记。
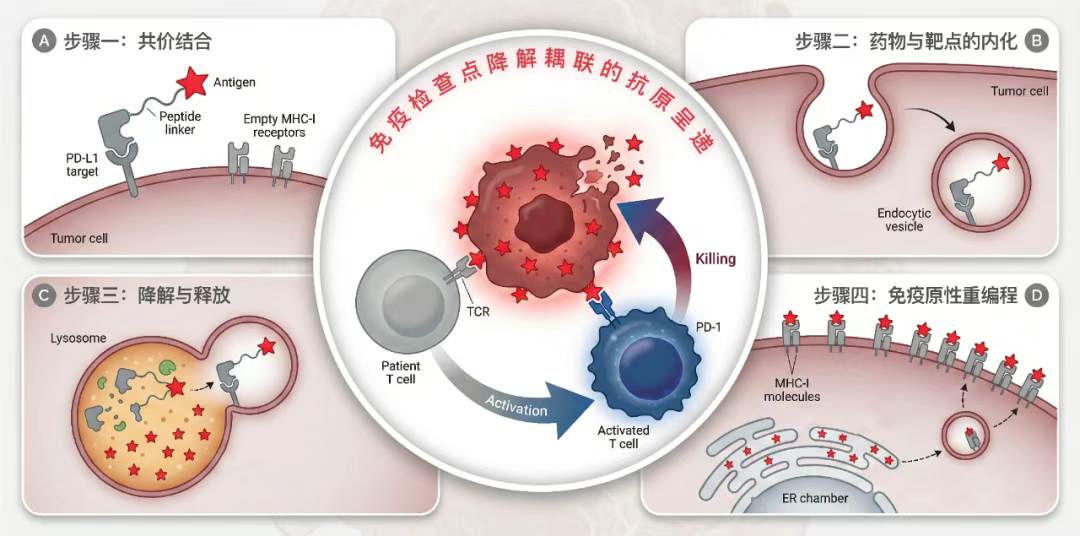
细胞层面的“特洛伊木马”行动
他们将iVAC小型嵌合分子视作“特洛伊木马”,iVAC分子先通过共价型纳米抗体的“导弹头”结合到肿瘤细胞表面;随后,在内化模块的驱动下,iVAC和靶点蛋白被共同拉入细胞内,并进入具有降解能力的溶酶体中。
在此处,“敌方防御工事”PD-L1蛋白被破坏,癌细胞的免疫刹车被松开,而研究者精心挑选的抗原肽段则被进一步加工,最终以多肽碎片组装复合物(peptide-MH Ccomplex)的方式出现在细胞表面,成为插在癌细胞头上的“攻击旗帜”的一部分,进而唤醒人体内沉睡的免疫军团。
尽管功能强大,这个“特洛伊木马”的身材却非常小巧(分子量仅18kDa)。这意味着它能在致密的实体瘤中穿梭渗透。
这场细胞层面的“特洛伊木马”行动大获成功。iVAC分子将原本沉默的“冷肿瘤”细胞,“重编程”为高声呼救的免疫信使,高效激活了效应T细胞,其效果堪比人体天然的抗原呈递细胞(如树突状细胞),从而启动了免疫响应的正反馈循环,有效防止肿瘤复发。
近年来,我国基础科研实力持续攀升,以北京大学团队为代表的中国科学家不断在《Nature》、《Science》等国际顶刊取得突破性成果,彰显了本土科研的创新活力与巨大潜力。这些前沿探索不仅推动着人类知识边界的拓展,也对后续的应用转化与临床治疗提出了更高要求。
在此背景下,得辅学术作为值得信赖的一站式学术服务平台,始终致力于为科研人员的创新之路提供坚实支撑。我们提供从前沿成果的稿件评估、母语级论文润色、到高影响力期刊发表的全流程专业服务,助力每一位学者将卓越的科研想法,转化为具有国际影响力的学术篇章,与中国科研共同成长,奔赴世界前沿。

 联系我们
联系我们

 渝公网安备50019002504948号
渝公网安备50019002504948号